| Nome Completo Oficial |
Fator de necrose tumoral humana recombinante-alfa / TNFSF2, variante (rHuTNF-alfa / TNFSF2, variante) |
| Sequência |
 |
| Sequência de Aminoácidos |
MRKRKPVAHV VANPQAEGQL QWLNRRANAL LANGVELRDN QLVVPSEGLY LIYSQVLFKG QGCPSTHVLL THTISRIAVS YQTKVNLLSA IKSPCQRETP EGAEAKPWYE PIYLGGVDFQL EKGDRLELDYFAQVLFKG |
| Sinônimos |
Fator de Necrose Tumoral, TNFSF2, Cachectina, Fator de Indução de Diferenciação (DIF), Necrose, Citotoxina |
| Número de acesso |
P01375 |
| Geneid. |
7124 |
| Resumo |
O uso clínico da potente atividade antitumoral do TNF-alfa tem sido limited pelos efeitos colaterais pró-inflamatórios, incluindo febre, hipotensão limitante da dose, hepatotoxicidade, trombose intravascular e hemorragia. O desenvolvimento de TNF-alfamutantes clinicamente aplicáveis com baixa toxicidade sistêmica tem sido um intenso interesse farmacológico. O TNF-alfa humano, que se liga ao TNF-R55 murino, mas não ao TNF-R75 murino, exibe atividade antitumoral retida e toxicidade sistêmica reduzida em camundongos em comparação com o TNF-alfa murino, que se liga a ambos os receptores de TNF murino. Com base nesses resultados, muitos TNF-alfamutantes que se ligam seletivamente ao TNF-R55 foram projetados. Esses mutantes exibiram atividades citotóxicas em linhas de células tumorais in vitro e exibiram menor toxicidade sistêmica in vivo. |
| fonte |
Escherichia coli. |
| Peso molecular |
Aproximadamente 16.9 kDa, uma única cadeia polipeptídica não glicosilada contendo 151 aminoácidos. Em comparação com o tipo selvagem, a variante de rHuTNF-α tem uma deleção de sequência de aminoácidos (aa) de aa 1-7, e o aa seguinte substitui Arg8, Lys9, Arg10 e Phe157 que se provou ter mais atividade e com menos lado inflamatório efeito in vivo. |
| Atividade biológica |
Totalmente biologicamente ativo quando comparado ao padrão. O ED50 conforme determinado por um ensaio de citotoxicidade usando células L929 murinas é inferior a 0.01 ng / ml, correspondendo a uma atividade específica de> 1.0 × 107 IU / mg na presença de actinomicina D. |
| Aparência |
Pó branco, esterilizado e liofilizado (liofilizado). |
| Formulação |
Liofilizado de uma solução concentrada filtrada de 0.2 um em PBS, pH 7.0. |
| Endotoxina |
Menos de 1 EU / ug de rHu TNF-α / TNFSF2, Variante conforme determinado pelo método LAL. |
| Reconstituição |
Recomendamos que este frasco seja centrifugado brevemente antes de abrir para trazer o conteúdo para o fundo. Reconstitua em água destilada estéril ou tampão aquoso contendo BSA 0.1% a uma concentração de 0.1-1.0 mg / mL. As soluções estoque devem ser distribuídas em alíquotas de trabalho e armazenadas a ≤ -20 ° C. Outras diluições devem ser feitas em soluções tamponadas apropriadas. |
| Estabilidade e Armazenamento |
Use um freezer de descongelamento manual e evite ciclos repetidos de congelamento-descongelamento.- 12 meses a partir da data de recebimento, -20 a -70 ° C conforme fornecido.- 1 mês, 2 a 8 ° C em condições estéreis após a reconstituição.- 3 meses, -20 a -70 ° C em condições estéreis após reconstituição. |
| Referências |
|
| SDS-PAGE |
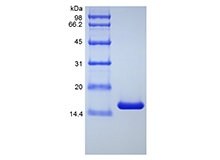 |
| Download da Folha de Dados de Segurança (SDS) |
Clique para fazer o download |
| Download da Folha de Dados Técnicos (TDS) |
Clique para fazer o download |



