| Nome Completo Oficial |
Fator inibidor de leucemia humana recombinante (rHuLIF) |
| Sequência |
 |
| Sequência de Aminoácidos |
SPLPITPVNA TCAIRHPCHN NLMNQIRSQL AQLNGSANAL FILYTAQGE PFPNNLDKLC GPNVTDFPPF HANGTEKAKL VELYRIVVYL GTSLGNITRD QKILNPSALS LHSKLNATAD ILRGLLSNVL CRLCSKYHVG HVDVTYGPDT SGKDVFQKKK LGCQLLGKYK QIIAVLAQAF |
| Sinônimos |
Fator de estimulação de diferenciação, fator D, inibidor de LPL derivado de melanoma, MLPLI |
| Número de acesso |
P15018 |
| Geneid. |
3976 |
| Resumo |
O fator inibidor da leucemia (LIF) é um membro da família da Interleucina 6. Essa proteína é expressa principalmente no trofectoderma do embrião em desenvolvimento, com seu receptor LIFR expresso em toda a massa celular interna. LIF tem a capacidade de induzir diferenciação terminal em células leucêmicas. Suas atividades incluem a indução da diferenciação hematopoiética em células normais e de leucemia mieloide, a indução da diferenciação de células neuronais e a estimulação da síntese protéica de fase aguda em hepatócitos. O LIF é usado em cultura de células-tronco embrionárias de camundongo, porque a remoção de LIF empurra as células-tronco em direção à diferenciação, mas elas retêm seu potencial proliferativo ou pluripotência. Também é usado em ensaios clínicos de fase II, que podem auxiliar na implantação de embriões em mulheres que não conseguiram engravidar apesar das tecnologias de reprodução assistida (ART). LIF humano maduro (180 aa) compartilha 78%, 82%, 91%, 88% e 87% de identidade de sequência aa com LIF de camundongo, rato, canino, bovino e suíno, respectivamente. |
| fonte |
Escherichia coli. |
| Peso molecular |
Aproximadamente 19.7 kDa, uma única cadeia polipeptídica não glicosilada contendo 180 aminoácidos. |
| Atividade biológica |
Totalmente biologicamente ativo quando comparado ao padrão. O ED50 conforme determinado pela proliferação dependente da dose de células TF-1 humanas é inferior a 0.1 ng / ml, correspondendo a uma atividade específica de> 1.0 × 107 IU / mg. |
| Aparência |
Pó branco, esterilizado e liofilizado (liofilizado). |
| Formulação |
Liofilizado de uma solução concentrada filtrada de 0.2 um em PBS, pH 7.4. |
| Endotoxina |
Menos de 1 EU / ug de rHuLIF conforme determinado pelo método LAL. |
| Reconstituição |
Recomendamos que este frasco seja centrifugado brevemente antes de abrir para trazer o conteúdo para o fundo. Reconstitua em água destilada estéril ou tampão aquoso contendo BSA 0.1% a uma concentração de 0.1-0.2 mg / mL. As soluções estoque devem ser distribuídas em alíquotas de trabalho e armazenadas a ≤ -20 ° C. Outras diluições devem ser feitas em soluções tamponadas apropriadas. |
| Estabilidade e Armazenamento |
Use um freezer de descongelamento manual e evite ciclos repetidos de congelamento-descongelamento.- 12 meses a partir da data de recebimento, -20 a -70 ° C conforme fornecido.- 1 mês, 2 a 8 ° C em condições estéreis após a reconstituição.- 3 meses, -20 a -70 ° C em condições estéreis após reconstituição. |
| Referências |
|
| SDS-PAGE |
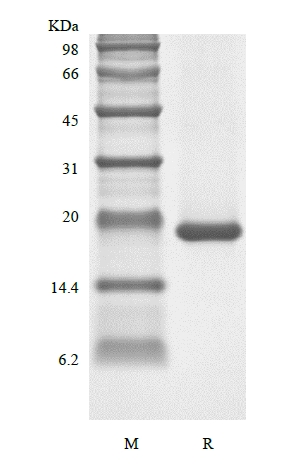 |
| Download da Folha de Dados de Segurança (SDS) |
Clique para fazer o download |
| Download da Folha de Dados Técnicos (TDS) |
Clique para fazer o download |



