| Nome Completo Oficial |
Fator de crescimento epidérmico humano recombinante (rHuEGF) |
| Sequência |
 |
| Sequência de Aminoácidos |
NSDSECPLSH DGYCLHDGVC MYIEALDKYA CNCVVGYIGE RCQYRDLKWW ELR |
| Sinônimos |
Urogastrona, URG |
| Número de acesso |
P01133 |
| Geneid. |
|
| Resumo |
O fator de crescimento epidérmico (EGF) foi originalmente descoberto em preparações brutas de fator de crescimento do nervo preparado a partir de glândulas submaxilares de camundongo como uma atividade que induzia a abertura precoce da pálpebra, erupção dos incisivos, inibição do crescimento do cabelo e retardo do crescimento quando injetado em camundongos recém-nascidos. O EGF humano foi isolado da urina com base no seu efeito inibitório na secreção gástrica e denominado urogastrona, em conformidade. O EGF é prototípico de uma família de fatores de crescimento derivados de precursores ancorados na membrana. Todos os membros desta família são caracterizados pela presença de pelo menos uma unidade estrutural EGF (definida pela presença de um motivo conservado de 6 cisteína que forma três ligações dissulfeto) em seu domínio extracelular. O EGF é inicialmente sintetizado como uma proteína transmembranar precursora de 130 kDa contendo 9 unidades de EGF. A sequência de EGF solúvel madura corresponde à unidade de EGF localizada próximo ao domínio transmembranar. O precursor do EGF de membrana é capaz de se ligar ao receptor do EGF e foi relatado como biologicamente ativo. EGF humano maduro compartilha 70% de identidade de sequência aa com EGF maduro de camundongo e rato. |
| fonte |
Escherichia coli. |
| Peso molecular |
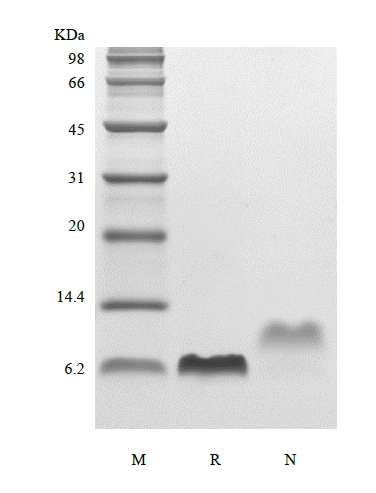
Aproximadamente 6.2 kDa, uma única cadeia polipeptídica não glicosilada contendo 53 aminoácidos. |
| Atividade biológica |
Totalmente biologicamente ativo quando comparado ao padrão. O ED50 conforme determinado por um ensaio de proliferação celular usando células Balb / c 3T3 murinas é inferior a 1 ng / ml, correspondendo a uma atividade específica de> 1.0 × 106 IU / mg. |
| Aparência |
Pó branco, esterilizado e liofilizado (liofilizado). |
| Formulação |
Liofilizado de uma solução concentrada filtrada de 0.2 um em PBS, pH 7.4. |
| Endotoxina |
Menos de 1 EU / ug de rHuEGF conforme determinado pelo método LAL. |
| Reconstituição |
Recomendamos que este frasco seja centrifugado brevemente antes de abrir para trazer o conteúdo para o fundo. Reconstitua em água destilada estéril ou tampão aquoso contendo BSA 0.1% a uma concentração de 0.1-1.0 mg / mL. As soluções estoque devem ser distribuídas em alíquotas de trabalho e armazenadas a ≤ -20 ° C. Outras diluições devem ser feitas em soluções tamponadas apropriadas. |
| Estabilidade e Armazenamento |
Use um freezer de descongelamento manual e evite ciclos repetidos de congelamento-descongelamento.- 12 meses a partir da data de recebimento, -20 a -70 ° C conforme fornecido.- 1 mês, 2 a 8 ° C em condições estéreis após a reconstituição.- 3 meses, -20 a -70 ° C em condições estéreis após reconstituição. |
| Referências |
|
| SDS-PAGE |
 |
| Download da Folha de Dados de Segurança (SDS) |
Clique para fazer o download |
| Download da Folha de Dados Técnicos (TDS) |
Clique para fazer o download |



